千人千例 | HR+/HER2-乳腺癌免疫治疗进展

前言
激素受体阳性,人表皮生长因子受体2阴性(HR+,HER2-)是乳腺癌中最常见的亚型,约占所有乳腺癌的70%[1]。尽管长期以来该亚型被认为对免疫治疗反应不佳,但随着研究的深入,一些新的探索开始关注免疫检查点抑制剂联合化疗对ER+/HER2-高危乳腺癌的疗效,进一步改善了HR+,HER2-乳腺癌患者的生存预后。今年ESMO年会上报道了两项关于早期HR+/HER-2阴性乳腺癌免疫治疗的Ⅲ期随机对照研究,正式开启了HR阳性、HER-2阴性乳腺癌免疫治疗新时代,成为了乳腺癌免疫治疗进展的一个重要节点。本文对这两项研究亮点进行解读。
CheckMate7FL 研究
CheckMate7FL是首个在早期高危雌激素受体(estrogen receptor,ER)阳性、HER-2阴性乳腺癌中评估纳武利尤单抗+新辅助化疗(neoadjuvant chemotherapy,NACT)+辅助内分泌治疗的前瞻性Ⅲ期随机试验[2]。
该研究患者以1∶1的比例随机接受NACT(紫杉醇+蒽环类药物+环磷酰胺)+纳武利尤单抗治疗(纳武利尤单抗+化疗组),或NACT+安慰剂治疗(安慰剂+化疗组),术后患者接受纳武利尤单抗(纳武利尤单抗+化疗组)或安慰剂(安慰剂+化疗组)+内分泌治疗。
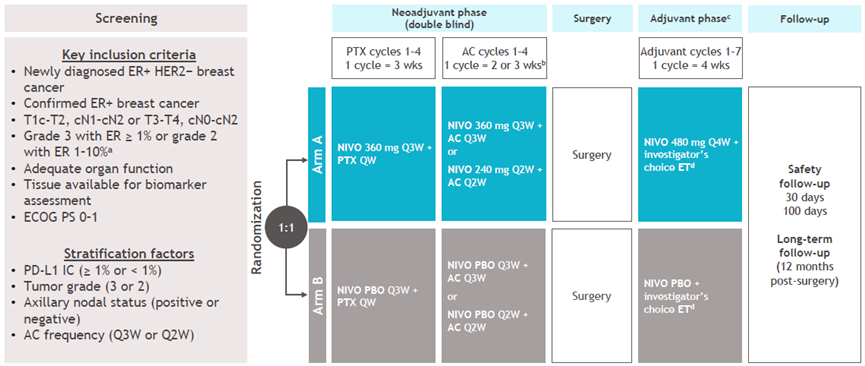
2023年ESMO年会上报道了该研究结果:纳武利尤单抗+化疗组的pCR率显著高于安慰剂+化疗组(24.5%∶13.8%,P=0.0021);亚组人群中纳武利尤单抗+化疗组患者的pCR率也显著高于安慰剂+化疗组(30.7%∶8.1%);PD-L1阳性患者中纳武利尤单抗带来显著pCR获益(44.3%∶20.2%)和残余癌症负担0、1级率总体改善(尤其是PD-L1阳性患者)。在该研究NACT阶段,纳武利尤单抗+化疗组和安慰剂+化疗组患者的3、4级TRAE发生率相似(35%∶32%),纳武利尤单抗+化疗组中2例死亡(肺炎、肝炎)与研究药物相关;纳武利尤单抗+化疗组免疫相关TRAE的发生率高于安慰剂+化疗组。与该研究单纯NACT相比,纳武利尤单抗联合NACT显著改善了早期高危ER+/HER-2-乳腺癌患者的pCR率和残余癌症负担0、1级率(尤其是PD-L1阳性的患者),但免疫相关TRAE发生率增加,总体安全性与纳武利尤单抗和化疗一致。
总的来说,CheckMate7FL的研究结果为ER+/HER2-高危乳腺癌患者提供了新的治疗前景。然而,我们需要更深入的研究来了解不同亚型患者的具体受益情况,并将这些发现转化为更个体化、精准的治疗策略。
KEYNOTE-756 研究
KEYNOTE-756研究是一项全球、Ⅲ期临床研究[3],旨在评估化疗±帕博利珠单抗新辅助治疗后内分泌治疗±帕博利珠单抗辅助治疗对早期高危ER阳性、HER-2阴性乳腺癌患者的疗效和安全性。
研究纳入1278例分期为T1c-2(≥2cm)cN1-2或T3-4 cN0-2、ER+/HER2-、乳腺浸润性导管癌3级患者,按1:1随机分为帕博利珠单抗组或安慰剂组。手术前帕博利珠单抗/安慰剂+紫杉醇(12周),随后接受帕博利珠单抗/安慰剂+多柔比星或表柔比星+环磷酰胺(4个周期),手术(±化疗)后接受帕博利珠单抗/安慰剂治疗+ET(9个周期)。主要终点是pCR(定义为ypT0/Tis ypN0,即乳腺原发灶无浸润性癌且区域淋巴结阴性)和无事件生存期(EFS),次要终点是总生存期(OS)、pCR(定义为ypT0 ypN0和ypT0/Tis,即乳腺和腋窝淋巴结无浸润性癌及原位癌,乳腺无浸润性癌)和安全性。
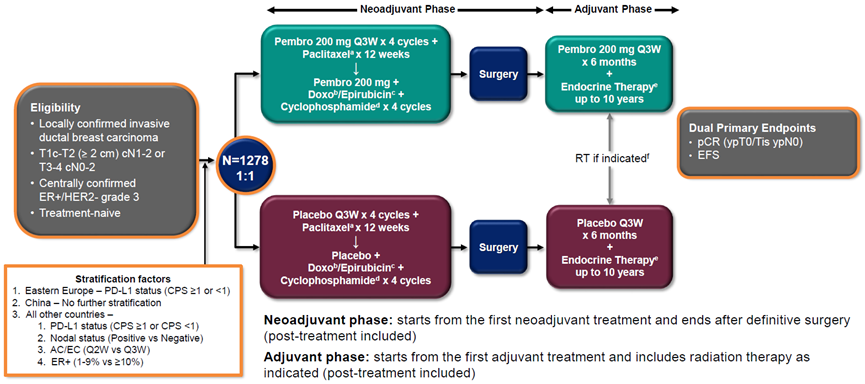
中位随访时间33.2个月时,帕博利珠单抗组和安慰剂组的pCR(ypT0/Tis ypN0)率分别为24.3%(95% CI, 21.0%-27.8%)和15.6% (95% CI, 12.8%-18.6%)。ypT0ypN0(21.3% vs. 12.8%)和ypT0/Tis(29.4% vs. 18.2%)的pCR率结果与主要终点结果一致。EFS数据尚不成熟。这意味着与安慰剂相比,帕博利珠单抗治疗ER+/HER2-乳腺癌患者具有更佳的临床获益。亚组的分析结果显示,帕博利珠单抗+化疗为不同亚组患者带来的pCR获益基本一致。然而需要指出的是,对于ER+/HER2-乳腺癌患者而言,pCR率的提高是否能转化为生存的获益依然值得进一步探讨,同时也期待该研究后续随访数据来揭示免疫治疗的加入是否可以为ER+/HER2-乳腺癌带来生存获益。
总结
综上所述,KEYNOTE-756研究及CheckMate-7FL研究打开了HR+/HER2-高危早期乳腺癌患者治疗的新视角,希望随着未来EFS结果的释出以及越来越多深入探索的开展,免疫治疗能够真正走入临床实践。
结语
乳腺癌诊疗的探索从未止步,“以患者为中心”,在免疫治疗前行之路上不断精进,勇往直前。为医疗领域高质量发展、为健康中国宏伟蓝图、为更多乳腺癌患者生存获益与可期未来,贡献“千人千例”的价值与力量!
参考文献:
1. Howlader N, Altekruse S, Li C. US incidence of breast cancer subtypes defined by joint hormone receptor and HER2 status. J Natl Cancer Inst. 2014;106(5).
2. LOI S, CURIGLIANO G, SALGADO R F, et al. LBA20 A randomized, double-blind trial of nivolumab (NIVO) vs placebo (PBO) with neoadjuvant chemotherapy (NACT) followed by adjuvant endocrine therapy (ET) ± NIVO in patients (pts) with high-risk, ER+ HER2− primary breast cancer (BC) [J]. Ann Oncol, 2023, 34: S1259-S1260.
3.CARDOSO F, MCARTHUR H L, SCHMID P, et al. LBA21 KEYNOTE-756: Phase III study of neoadjuvant pembrolizumab (pembro) or placebo (pbo) + chemotherapy (chemo), followed by adjuvant pembro or pbo+ endocrine therapy (ET) for early-stage high-risk ER+/HER2– breast cancer [J]. Ann Oncol, 2023, 34: S1260-S1.