
殷咏梅
主任医师
摘要:肿瘤的治疗中化疗是一个关键方式,但化疗往往是一把“双刃剑”,常常“敌我不分”。对许多接受化疗的患者来说,化疗带来的不良反应、痛苦甚至死亡使他们对继续治疗望而却步,因此,减轻化疗的不良反应在癌症治疗中具有重大意义。抗肿瘤药物的不良反应、发生机制和类型:1)胃肠道反应:主要是恶心和呕吐,属于可逆性的不良反应;2)血液学毒性:白细胞下降、血小板下降以及贫血等,属于可逆性的不良反应;3)心脏毒性:可引起患者生命危险,为不可逆性的不良反应。
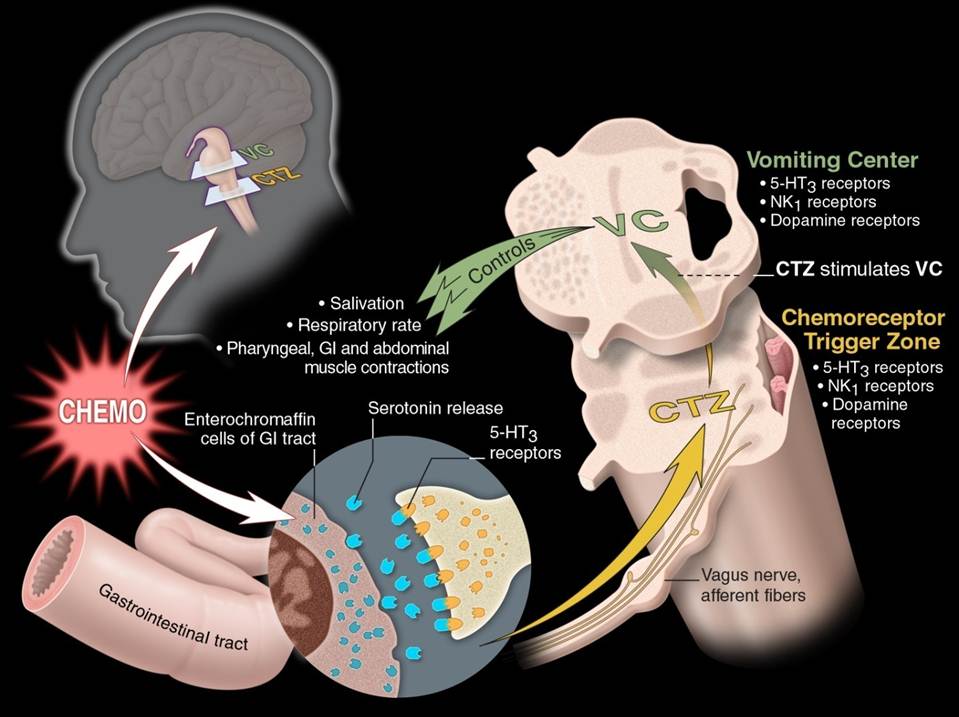
临床上,将伴随肿瘤化疗发生的恶心呕吐定义为化疗相关性恶心呕(Chemotherapy-Induced Nausea and Vomiting,CINV)。化疗导致恶心呕吐反应的发生机制异常复杂,至今仍未彻底阐明。目前一般认为CINV主要通过以下途径引起:1)抗肿瘤药物进入人体后刺激胃肠道,尤其是嗜铬细胞释放神经递质5-HT,5-HT与相应受体结合产生的神经冲动,由迷走神经和交感神经传入呕吐中枢而导致呕吐。2)抗肿瘤药物及其代谢产物直接刺激延髓的化学感受器 (CTZ) ,进而传递至呕吐中枢引发呕吐。3)感觉、神经因子等直接刺激大脑皮质通路导致呕吐,此类多见于预期性CINV。
根据发生时间和处理方式的不同,可将CINV分为3种类型:1)急性呕吐:用药后数分钟到数小时内出现,一般在用药后5~6小时呕吐达最高峰,24小时内缓解。2)迟发性呕吐: 用药后24小时后出现,如DDP引起的迟发性呕吐常于给药后48-72 小时达最高峰,可持续6-7天。3)预期性呕吐:属条件反射,是指在前一次化疗中出现恶心/呕吐的病人,在下一次化疗开始前就出现恶心/呕吐,发生率为18-57%,常以恶心为主,年轻人的发生率高于老年人。
为预防恶心呕吐的发生,行肿瘤治疗前应充分评估,以针对患者可能出现的呕吐制定个体化的治疗方案。
肿瘤化疗的血液毒性一般表现为中性粒细胞减少、血小板减少和贫血等。处理原则包括密切观察白细胞减少的动态变化,定期检测血像,如紫杉醇和培美曲塞使用前,都需要使用激素进行预处理。
值得注意的是,激素药物进入人体后,在24小时甚至36~48小时内血常规检查显示白细胞未必会下降甚至出现升高的现象,这是由于使用激素类药物所造成的一种假象,但是在随后的2~4天,患者的白细胞会急剧下降。因此,我们要定期检测患者的血象,以防止在第一次使用化疗药物后24小时造成患者的血象因激素而升高的假象,从而忽略以后对患者血常规的动态观察。
当出现白细胞下降明显,必要时可给予粒细胞集落刺激因子(G-CSF)提升白细胞治疗。而对于出现四度骨髓抑制的患者,需要减少本周期或下一周期的化疗药物剂量或者停药予以纠正。对于曾经出现白细胞严重下降的、四度骨髓抑制的患者,可能会出现粒缺性发热,应注意预防感染,必要时给予抗生素治疗。
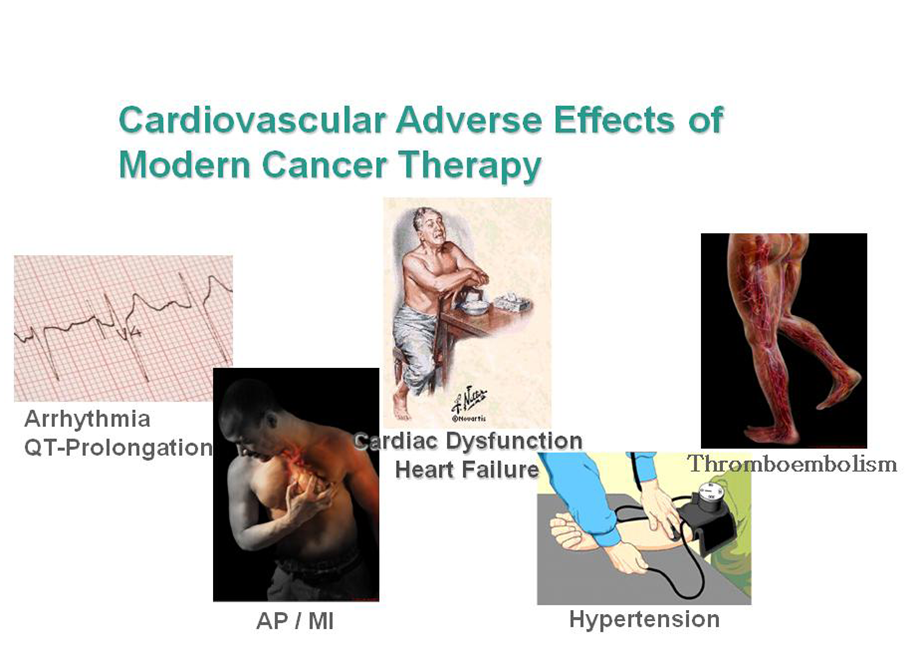
研究显示,在1962-2001年间1713例发生癌症的患者中,心脏异常的发生率为56.4%。癌症幸存者因心脏疾病死亡的发生率是同龄对照者的8-10倍。欧洲肿瘤中心1995年癌症患者心脏会诊比例为7%,2008年该数字上升至77%,显示肿瘤治疗过程中心脏不良反应越来越受到重视。为解决肿瘤患者化疗的心脏毒性,欧洲成立了一个由肿瘤科和心脏科专家共同合作的新学科——肿瘤心脏病学(Cardio-Oncology)。
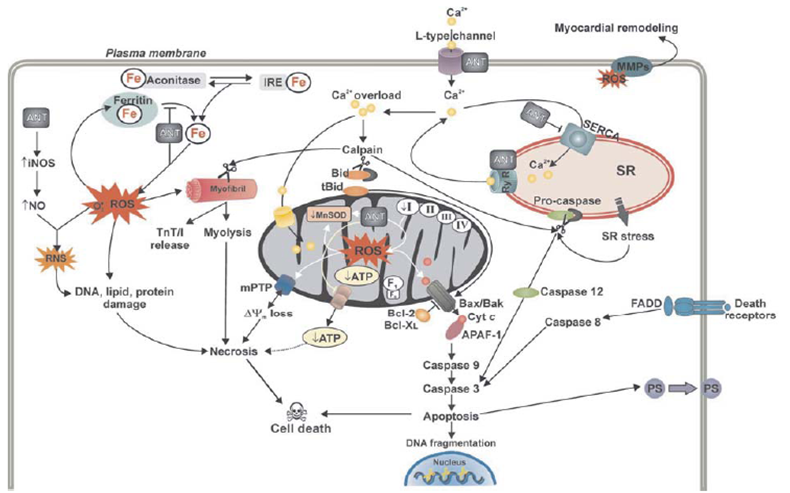
根据中国临床肿瘤学会和中华医学会血液学分会联合制定的《蒽环类药物心脏毒性防治指南(2013版)》介绍,蒽环类药物导致心脏毒性的机制目前尚未明了,目前比较成熟的是“自由基理论”。主要机制是,“铁介导的活性氧簇(ROS)的产生及促进心肌的氧化应激;蒽环类药物螯合铁离子后触发氧自由基,尤其是羟自由基的大量生成,导致心肌细胞膜脂质过氧化和心肌线粒体DNA的损伤等”。
根据蒽环类药物心脏毒性的发生时间,分为急性、慢性和迟发型三种类型。蒽环急性心脏毒性一般发生在给药后的几小时或几天内,在电生理方面表现比较早,一般表现为传导阻滞或心律失常的改变。慢性毒性发生在化疗后的1年内,而迟发型心脏毒性可能在化疗后的数年发生,对于这类患者,需要仔细询问病史,确定在过去的一些年间是否使用过蒽环类药物,以判断是否是因蒽环类的药物引起迟发性的心脏毒性。
对于蒽环类药物心脏毒性的监测,临床可用一些血液学指标或辅助检查等方式进行。主要有:1)肌钙蛋白I/T(cTnI/T):是心脏毒性早期的监测指标,能反映早期心肌细胞受到损伤。2)脑钠肽(BNP):反映心脏功能的一个指标,可先于心超结构变化之前出现异常,对于中长期的心功能监测具有重要的意义。3)辅助检查:超声心动图可判断心脏结构上的改变,用于心功能不全的诊断,对于使用赫赛汀和蒽环类药物的患者,每隔三个月检测一次左室射血分数是否达到警戒值,对减少药量或停药的处理有决定性的指导作用。此外,放射性核素心室显像(MUGA)可评估局部心室壁的运动和舒张功能,心肌磁共振成像(MRI)是评估心肌功能与损伤的有价值的工具,都可用于蒽环类药物心脏毒性的监测。
在预防蒽环类药物心脏毒性方面,国内外多个指南及规范,如《NCCN临床实践指南:非霍奇金淋巴瘤》、《NCCN临床实践指南:老年人肿瘤》、《ACC/AHA成人慢性心力衰竭诊断治疗指南(2013)》、《德国晚期转移性乳腺癌指南》、《蒽环类药物心脏毒性防治指南(2013版)》、《中国急性早幼粒细胞白血病诊疗指南(2014年版)》以及《中国抗癌协会乳腺癌诊治指南与规范(2015版)》均推荐右丙亚胺(DZR)作为蒽环类药物的心脏毒性保护剂,首次使用蒽环类药物就应联合使用右丙亚胺,以达到有效预防蒽环类药物心脏毒性的效果。
右丙亚胺自上市以来,价格便宜且能实实在在解决临床问题,多年来大量的循证医学研究都显示,右丙亚胺具有非常好的心脏保护作用。
一项关于右丙亚胺对以蒽环类为基础化疗的进展期/转移性乳腺癌患者的心脏保护作用的多中心随机对照Ⅲ期试验,164例入组的乳腺癌患者,随机分为单纯蒽环化疗组和联用右丙亚胺组。右丙亚胺与阿霉素的剂量比为20:1,与表阿霉素的剂量比为10:1。第1次应用蒽环即联合应用右丙亚胺,采用心超、心电图、CT等方法评估心脏功能及抗肿瘤疗效。
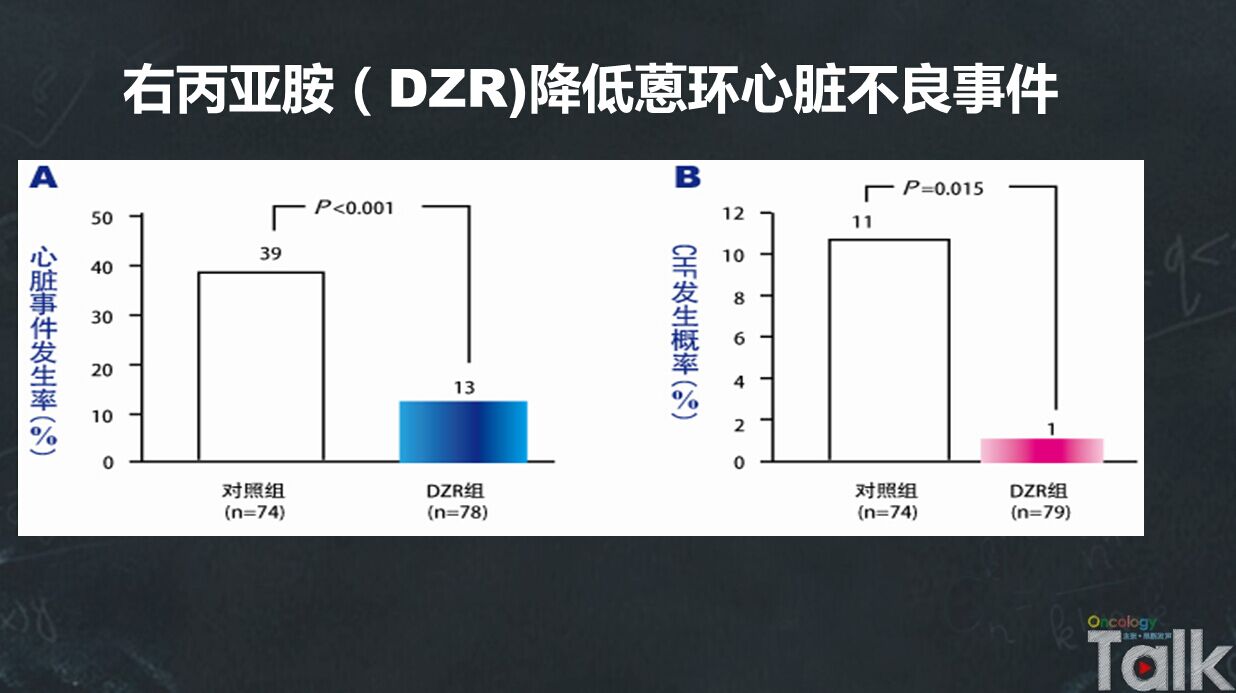
试验结果显示:单纯蒽环化疗组心脏事件的发生率为39%,而联用右丙亚胺组的发生率为13%,具有统计学差异;另外充血性心衰的发生率单纯化疗组为11%,联用右丙亚胺组为1%,差异也非常显著。说明单纯化疗组的心脏不良事件明显高于右丙亚胺组,右丙亚胺可明显降低心脏事件发生率。
一项长达10年的回顾性历史研究,分析评价了1993-2003年的318名乳腺癌患者使用右丙亚胺的心脏保护效果,其中绝大多数为早期乳腺癌,给予辅助化疗和/或姑息性化疗。对于心脏不良事件的监测采用心电图和心超的检查方法。
研究发现,多数患者接受了易发心脏不良事件的蒽环累积剂量,如87.4%的患者阿霉素累积剂量达到了200-400mg/m2,85.3%的患者表阿霉素累积剂量达到了400-600mg/m2。如果没有联合应用右丙亚胺,这些患者大部分将发生心脏不良事件,并因此可能需要更换治疗方案。本研究中只有5个病人(发生率1.6%)发生了有临床症状的充血性心衰(CHF),对比既往的单纯化疗的8-24%的CHF发生率,差异显著,说明右丙亚胺具有良好的心脏保护效果。
右丙亚胺使用方法及注意事项:1)使用时间:第1次使用蒽环类药物前联合应用DZR,可以有效预防蒽环类药物心脏毒性。2)使用剂量:DZR与蒽环类药物的剂量比为10-20:1,推荐DZR:ADM=20:1,DZR:DNR=20:1,DZR:EPI=10:1,DZR:MIT=50:1,DZR:PLD=10:1,DZR:THP=15:1。3)使用方法:用专用溶媒乳酸钠配置后,再用0.9%氯化钠或5%葡萄糖注射液稀释至200ml,快速静脉滴注,30分钟内滴完,滴完后即刻给予蒽环类药物。如果没有采取预防措施,患者出现了心功能不全、心律失常,甚至心衰、血栓等更严重的心脏毒副反应,需要及时请心脏科医生会诊,并对症处理。
最后,建议肿瘤内科医生与心脏科专家联合起来,为患者制定更合理的个体化治疗方案,以帮助患者安全度过化疗期间。